TIROIDITE
La tiroidite è un processo infiammatorio della tiroide. Esistono, tuttavia, diversi tipi di tiroidite che per prevalenza, decorso clinico e caratteristiche di laboratorio, si differenziano una dall’altra. La tiroidite acuta è una infiammazione di tipo granulocitario, la subacuta di tipo granulomatoso, la cronica di tipo linfocitario. La tiroidite acuta è molto rara e dovuta ad infezioni batteriche, la tiroidite subacuta è di origine virale. Entrambe sono solitamente transitorie e guariscono con la restituito ad integrum della tiroide.
La tiroidite cronica, invece, ha una eziologia sconosciuta, con patogenesi autoimmune, ed ha una varietà di manifestazioni cliniche che rispecchiano l’evoluzione del processo infiammatorio della ghiandola. Spesso i pazienti con tiroidite cronica hanno altre malattie autoimmuni associate e nella famiglia esistono altri casi di tireopatie autoimmuni. Predilige soprattutto le donne anziane ma anche donne più giovani nel periodo successivo alla gravidanza. Le tiroiditi croniche, inoltre, possono avere anche altre caratteristiche, comparire dopo una gravidanza ed essere scatenate dall’uso di determinati farmaci.
Pertanto le tiroiditi possono essere classificate in:
Tiroiditi acute:
Tiroidite batterica
Tiroidite parassitaria
Tiroiditi sub-acute:
Tiroidite di De Quervain
Tiroiditi croniche:
Tiroidite cronica Hashimoto
Tiroidite silente sporadica
Tiroidite silente post-partum
Tiroidite fibrosa di Riedel
Tiroidite da farmaci
TIROIDITE ACUTA
Epidemiologia
La tiroide ha delle caratteristiche anatomiche, quali una capsula protettiva, una ricca vascolarizzazione, e un efficiente sistema di drenaggio che limitano la diffusione del processo infettivo suppurativo. Per questo motivo e per la notevole diffusione degli antibiotici, la tiroidite acuta è un evento molto raro.
Eziopatogenesi
Spesso, infatti, colpisce soggetti giovani o addirittura molto giovani in cui, per la presenza di tiroidite recidivanti, va sospettata la presenza di residuo del dotto tireoglosso o la presenza di fistole del seno piriforme (spesso il sinistro nel 90% dei casi). Negli adulti, invece, il processo infettivo si propaga piu’ probabilmente per contiguità (faringiti, tonsilliti, parotiti, mastoiditi), per via ematogena (erisipela, infezioni pleuropolmonari, genitourinarie e gastrointestinali) o tramite ferite del collo.
Gli agenti batterici piu’ frequentemente coinvolti sono lo Staphylococcus Aureus, Streptocuccus pyogenes, Pneumococcus pneumonite, Enterobatteri, Batteri anaerobi, Funghi, Echinococcus granulosus e Pneumocistis carinii (in pazienti con AIDS).
Anatomia patologica
Nella tiroidite acuta l’infiammazione è caratterizzata da infiltrato di polimorfonucleati e linfociti associati a necrosi tissutale. A volte possono essere presenti dei veri e propri ascessi.
Clinica
La presenza di una tumefazione del collo, con la cute sovrastante calda e arrossata, sono tipici. Spesso è presente febbre con adenopatia laterocervicale satellite. Le complicanze sono rare.
Diagnosi
E’ presente leucocitosi neutrofila, mentre nelle parassitosi è presente eosinofilia. La VES e gli indici di infiammazione sono elevati; l’emocoltura può essere positiva nel caso di setticemia. La funzione tiroidea è solitamente nella norma.
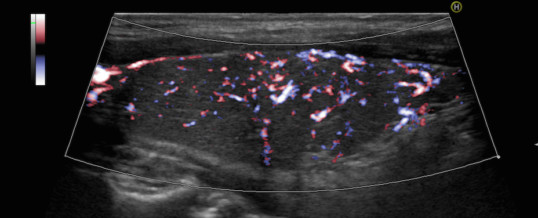
L’ecografia può riscontrare un’area anecogena corrispondente alla raccolta ascessuale (prenota un’ecografia tiroidea). La scintigrafia mostra un’area di ipocaptazione in corrispondenza dell’area infiammata. La captazione dello I 131 è ridotta nel 40% dei casi.
L’agoaspirato è utile nella identificazione dell’agente eziologico, mentre va evitato nel caso si sospetti una cisti da echinococco per evitarne la rottura (prenota un agoaspirato tiroideo). Può essere utile effettuare un esame radiologico mirato alla ricerca di eventuali fistole.
Terapia
La terapia richiede l’impiego di antibiotici a largo spettro o specifici in base all’antibiogramma del germe isolato dalla ghiandola. A volte puo’ essere utile il drenaggio della raccolta ascessuale. Importante iniziare il trattamento tempestivamente per evitare la diffusione del processo infiammatorio.
Se trattata tempestivamente non residua nessuna alterazione permanente della funzione tiroidea. Se il processo infiammatorio è così esteso da far residuare un ipotiroidismo, può essere necessario un trattamento con dosi sostitutive di levotiroxina (LT4).
TIROIDITE SUB-ACUTA
La tiroidite sub acuta, detta anche granulomatosa, o tiroidite di De Quervain, è caratterizzata solitamente da un risoluzione spontanea.
Per l’andamento clinico anche la tiroidite silente e la tiroidite post partum vengono considerate da alcuni autori delle tiroiditi sub-acute. In realtà il meccanismo eziopatogenetico è differente e sono da considerare delle varianti della tiroidite autoimmune. (Prenota una visita endocrinologica).
Epidemiologia
E’ piu’ frequente nelle donne (F/M=3-6/1), ha spesso un andamento stagionale con maggior frequenza nel periodo estivo-autunnale.
Eziopatogenesi
Anche se, spesso, non vengono trovati indici di infezione virale, la tiroidite sub-acuta ha un’origine virale, poichè a) si manifesta spesso in concomitanza con epidemie virali; b) è preceduta da un’infezione delle prime vie respiratorie; c) il paziente spesso lamenta sintomi prodromici quali astenia, mialgia, febbre.
Il processo infiammatorio si risolve, solitamente, con la restituito ad integrum.
I virus più frequentemente coinvolti sono Echovirus, Virus influenzali, Coxsackie A e B, Adenovirus, Epstein Barr, Virus della parotite etc..
Possono riscontrarsi occasionalmente degli anticorpi anti tiroide che non hanno, però, un ruolo nella patogenesi della malattia ma ne rappresentano un epifenomeno.
Anatomia patologica
E’ presente una infiltrazione di cellule infiammatorie (neutrofili e linfociti), i follicoli tiroidei diventano iperplastici con rottura dello strato epiteliale e spesso si osservano cellule giganti multinucleate attorno ai follicoli che, racchiudendo i residui di colloide fanno assumere al processo infiammatorio un aspetto di tipo granulomatoso. Con il tempo l’infiammazione lascia il posto ad una fibrosi di grado variabile, ma la restituito ad integrum finale e’solitamente completa.
Clinica
La durata della malattia è di circa 2-5 mesi e recidive sono presenti nel 20-35% dei pazienti. Il quadro clinico è spesso variabile.
Caratteristica e’ la presenza di dolore spontaneo e continuo (tiroidite pain full) nella regione anteriore del collo o che si irradia lateralmente alla mandibola o all’orecchio. Il dolore può essere così forte da impedire addirittura la palpazione della ghiandola.
A volte può essere avvertita una tumefazione tiroidea monolaterale che poi tende a migrare contro lateralmente (tiroidite migrante). Può essere presente febbre, solitamente moderata.
Nel 50% dei casi nella fase iniziale può presentarsi una tireotossicosi causata dal rilascio egli ormoni tiroidei da parte del tessuto tiroideo danneggiato dal processo infiammatorio, con un quadro di ipertiroidismo più o meno sfumato. (Prenota una visita endocrinologica).
Diagnosi
Si riscontra un innalzamento degli indici infiammatori (VES, PCR), i globuli bianchi sono normali o è presente una lieve leucocitosi con linfocitosi relativa.
Anticorpi anti tiroide possono essere presenti, a basso titolo e transitoriamente, nelle fasi iniziali della tiroidite sub acuta, anche se non sembrano avere un ruolo nella patogenesi del processo infiammatorio; la loro presenza è semplicemente un epifenomeno. Possono permanere livelli elevati di anticorpi se è presente una sottostante tiroidite di Hashimoto.
Il dosaggio degli anticorpi tiroidei e la clinica hanno un caratteristico andamento trifasico:
I fase di tireotossicosi: dura circa 4-6 settimane ed è caratterizzata dall’aumento in circolo di FT3, FT4 e Tg, rilasciati dai follicoli danneggiati dall’infiammazione, con soppressione del TSH. La scintigrafia, pertanto, rivela una ridotta captazione da parte della tiroide sia per il danno subito dai tireociti, sia per la mancata stimolazione da parte del TSH inibito. All’ecografia sono evidenti aree piu’ o meno ampie di ipoecogenicità.
II fase di ipotiroidismo transitorio: dura 2-8 settimane ed è caratterizzata da livelli di ormoni tiroidei ridotti (la tiroide in questa fase è più impegnata in processi riparativi che di neosintesi degli ormoni tiroidei) e da TSH aumentato. Spesso si tratta di ipotiroidismo subclinico.
III fase di restituito ad integrum: i parametri funzionali della tiroide ritornano nella norma.
In alcuni casi la ripresa funzionale può non avvenire e può residuare un ipotiroidismo permanente relato ad una estesa fibrosi successiva al processo infiammatorio o ad una concomitante tiroidite cronica. (Prenota una visita endocrinologica).
Terapia
La terapia è sintomatica e mira alla risoluzione del processo infiammatorio.
I farmaci piu’ utilizzati sono i corticosteroidi che determinano una risoluzione della sintomatologia (febbre, dolore) già dopo 1-2 giorni; la risposta ai FANS, invece, è solitamente più tardiva e caratterizzata da un aumento del numero di recidive e pertanto ad essa si preferisce la terapia con cortisonici.
E’ indicato iniziare con dosi elevate di prednisone (30-60 mg/die) (o dosi equivalenti di altri steroidi) per una settimana e poi scalare lentamente la posologia a 10-20 mg/die nelle settimane successive. La dose giornaliera deve essere ridotta gradualmente così da ridurre al minimo la possibilità di recidiva. In caso di recidiva è necessario ricominciare al terapia corticosteroidea a dosaggio pieno. La durata complessiva del trattamento non deve essere inferiore alle 6 settimane.
I cortisonici, pur avendo un notevole effetto sui sintomi e riducendo la sintomatologia dolorosa già 24-48 ore dopo l’inizio della terapia, non modificano significativamente il decorso reale della malattia.
Nei pazienti con controindicazioni all’uso di cortisonici si suggerisce l’uso di FANS per os (2.3 g/die suddivisi in tre quattro somministrazioni).
La tireotossicosi presente nella prima fase nella maggior pare dei casi non necessita di trattamento; altrimenti puo’ essere utile l’uso di beta-bloccanti per via orale.
E’ assolutamente inutile l’uso di tireostatici in quanto la tireotossicosi non è sostenuta da una aumentata produzione di ormoni tiroidei ma dalla liberazione di quelli preformati e contenuti nella colloide dei follicoli distrutti dal processo infiammatorio.
L’ipotiroidismo transitorio presente nella seconda fase non necessita solitamente di trattamento con LT4. Nei rari casi (5%) in vi è evoluzione verso un ipotiroidismo permanente puo’ essere necessario trattamento sostitutivo con levotiroxina.
Dopo 3 mesi dall’inizio del trattamento steroideo o comunque dopo un mese dalla sua sospensione è necessario eseguire un controllo di FT3, FT4, TSH, degli indici di flogosi ed una ecografia della tiroide. Ricontrollare successivamente questi parametri dopo 6 o 12 mesi. (Prenota una visita endocrinologica).
TIROIDITI CRONICHE
TIROIDITE CRONICA DI HASHIMOTO
Si caratterizza per una cronica infiltrazione linfocitaria che porta spesso ad una progressiva e irreversibile ipofunzione della tiroide.
Epidemiologia
E’ la più frequente delle patologie tiroidee ed è la causa più frequente di ipotiroidismo nelle aree del mondo con un sufficiente apporto di iodio, mentre nelle aree a carenza iodica la tiroidite cronica e’ ancora oggi una malattia relativamente rara.
Nelle donne l’incidenza è di 3,5 casi per 1000 abitanti l’anno negli uomini, invece, è più bassa (0,8 casi per 1000 abitanti l’anno). La differente distribuzione tra i sessi è meno evidente per la variante fibrosa.
Fisiopatologia
Alla base della patologia vi è un processo infiammatorio autoimmune che porta alla distruzione dei follicoli. Sia l’immunità cellulo-mediata che anticorpo-mediata sono chiamate in causa nella patogenesi della malattia.
Le cellule infiammatorie predominanti nel tessuto tiroideo sono linfociti B e T. I linfociti T helper vengono attivati contro le cellule tiroidee. Il meccanismo di attivazione dei linfociti non è noto ma, probabilmente, può avvenire per microchimerismo molecolare da parte di agenti esogeni o per attivazione diretta da parte di tireociti che espongono, in modo aberrante sulla superficie cellulare, delle molecole in grado di provocare l’ attivazione dei linfociti. Una volta attivato, il linfocita T helper produce diverse citochine che perpetuano e rendono cronico il processo infiammatorio autoimmune.
Alcune di queste citochine inducono, tra l’altro, l’espressione di fas sulle cellule tiroidee. E poichè i linfociti T citotossici esprimono in superficie il fas ligand, quest’ultimo, interagendo con il fas espresso dai tireociti, determina la morte apoptotica dei tireociti.
Quindi, il processo infiammatorio e l’infiltrazione linfocitaria (da cui il nome di tiroidite linfocitica) determinano una riduzione della sintesi degli ormoni tiroidei, tramite la distruzione apoptotica delle cellule tiroidee. Si determina così, contemporaneamente, una riduzione della capacità di organificare lo iodio intratiroideo e un rilascio di iodioproteine (tireoglobulina) da parte dei tireociti lisati.
Tuttavia, affinchè si manifesti l’ipotiroidismo, è necessaria la distruzione di almeno il 90% del tessuto tiroideo.
Il meccanismo umorale, invece sembra avere un ruolo di secondo piano. Infatti, a differenza di quanto accade in vitro, gli anticorpi anti TPO sembrano incapaci di produrre un danno al tireocita in vivo. Inoltre, a conferma di ciò, gli anticorpi anti TPO che passano la placenta dalla madre al feto non provocano alcun danno alla tiroide fetale. Gli anticorpi anti TSH-R bloccanti, al contrario, possono bloccare transitoriamente anche la tiroide fetale, suggerendo l’ ipotesi che possano avere un ruolo di primaria importanza nella patogenesi delle tiroiditi autoimmuni.
Classicamente gli autoanticorpi che si riscontrano nella tiroidite cronica sono quelli anti tireoperossidasi (Ab anti-TPO) (95%) e anti tireoglobulina (Ab anti-Tg) (50-60%).
Possono occasionalmente comparire anche degli anticorpi anti TSH-recettore bloccanti (TSHR blocking Ab), responsabili della variante atrofica (detta mixedema idiopatico o morbo di Gull) o ancora piuùraramente anticorpi anti TSH-recettore stimolanti (TSHRAb), responsabili del transitorio, o a volte permanente, ipertiroidismo che raramente è stato riscontrato in pazienti affetti da tiroidite di Hashimoto (hashitossicosi o ipertiroidite).
Anatomia patologica
Il quadro istologico può variare in base all’ estensione e all’ entità del processo infiammatorio ma è sostanzialmente caratterizzato da un diffuso infiltrato linfocitario, che in alcuni casi possono formare dei tipici follicoli linfoidi con tanto di centro germinale. Il grado di infiltrazione linfocitaria correla con il livello di anticorpi circolanti. La colloide è spesso sparsa. Si osserva tra l’altro fibrosi, soprattutto nelle tiroiditi di vecchia data, e obliterazione dei follicoli tiroidei. Frequente è la rottura della membrana basale follicolare e la distruzione dei tireociti, mentre le restanti cellule epiteliali sono solitamente piu’ grandi della norma, chiare, mostrano la presenza di strutture ossifile nel citoplasma (mitocondri), sono chiamate cellule Askanazy, e sono patognomoniche della tiroidite cronica.
Istologicamente possono essere distinte due varianti:
1) Variante ossifila: si caratterizza per la prevalenza di cellule ossifile, per una prevalenza dell’ infiltrazione linfocitaria con formazione di follicoli rispetto alla fibrosi;
2) Variante fibrosa: l’infiltrato è costituito prevalentemente da plasmacellule e la fibrosi è prevalente, e per tanto ha una maggior probabilità di sfociare in ipotiroidismo. Questa forma raggiunge la sua massima espressione nel mixedema idiopatico dell’adulto.
Il meccanismo eziopatogenetico alla base delle due forme sembra essere, però, lo stesso.
Fattori di rischio
– Genetici: è dimostrata una associazione significativa tra la tiroidite di Hashimoto e alcuni antigeni di istocompatibilità (HLA-DR, HLA-DR5 e alcuni alleli di DQ).
Inoltre la tiroidite di Hashimoto insorge con maggior frequenza in soggetti affetti da sindrome di Down o con disgenesia gonadica (Turner, Klinefelter), (prenota una cariotipo) facendo supporre che altri geni possano essere coinvolti nella patogenesi.
Probabilmente, però, alla base dello sviluppo della tiroidite autoimmune vi è una suscettibilità poligenica in cui si possono chiamare in causa anche geni non HLA-relati; per esempio determinati polimorfismi del gene CTLA4 sono associati alla possibilità di sviluppare anticorpi antitiroide.
– Gravidanza: una percentuale variabile dall’8% al 10% delle donne in gravidanza sviluppa una tiroidite autoimmune che ha le stesse caratteristiche della tiroidite di Hashimoto dalla quale si differenzia solamente per l’ aspetto transitorio.
– Iodio e sostanze contenenti iodio: queste hanno la capacità di far precipitare un processo autoimmune nei soggetti predisposti. Il meccanismo di questo fenomeno non è ancora molto chiaro, ma si pensa che l’aumentato grado di iodazione della tireoglobulina aumenti anche la sua antigenicità, così come molti peptidi responsabili della risposta immune linfocitaria sono molto più antigenici quando sono iodati.
– Citochine: il trattamento con IL-2 o interferone a può precipitare la comparsa della patologia autoimmune, soprattutto in soggetti predisposti.
– Irradiazione: la comparsa di anticorpi antitiroide avviene molto più frequentemente dopo l’esposizione a basse dosi radiazioni, come si è visto dopo il disastro di Chernobyl.
– Età: la prevalenza della patologia tende ad aumentare con l’età.
– Sesso: la prevalenza della patologia è maggiore nel sesso femminile e quindi probabilmente fattori ormonali possono concorrere alla patogenesi di questa patologia autoimmune.
– Infezioni: non ci sono evidenze dirette che infezioni causino tiroiditi autoimmuni negli esseri umani. Negli animali, però, diverse infezioni virali possono precipitare una tiroidite autoimmune. Inoltre si è visto che in pazienti con pregressa tiroidite sub-acuta si può sviluppare a lungo termine una disfunzione autoimmune tiroidea, come se un insulto di tipo infettivo sia necessario per precipitare l’autoimmunità tiroidea in soggetti predisposti.
Occorre comunque tenere ben distinti i fattori eziopatogenetici, in grado di modificare la risposta immune, da quelli non patogeneticci che invece sono in grado, solamente, di slatentizzare la malattia.
Clinica
Frequente è la comparsa di gozzo, che avviene solitamente in modo graduale, indolente senza provocare disturbi al paziente, e sebbene lo sviluppo di atrofia tiroidea dovrebbe essere il risultato finale della distruzione autoimmune della ghiandola, la progressione del gozzo verso lo stato atrofico non è di così comune riscontro.
In conclusione, quindi, il volume tiroideo può essere aumentato (gozzo), come avviene nella maggior parte dei casi, normale o ridotto come avviene nella forma atrofica. (Prenota una visita endocrinologica).
Nella tiroidite di Hashimoto si possono riscontrare diverse situazioni funzionali:
1) normale funzione tiroidea; 2) ipotiroidismo subclinico; 3) ipotiroidismo clinico; 4) ipertiroidismo transitorio.
La storia naturale della tiroidite cronica è, solitamente, caratterizzata da una lenta progressione verso l’ipotiroidismo clinico e tale progressione è maggiore nei maschi che nelle femmine, anche se altri fattori intercorrenti possono interferire e modificare il decorso della storia naturale della patologia.
Spesso i pazienti sono asintomatici, se si esclude la presenza di un lieve gozzo. Nel paziente da lungo tempo affetto da tiroidite cronica, invece, i disturbi clinici avverti sono quelli tipici dell’ ipotiroidismo. Rara, anche se possibile, è a comparsa di ipertiroidismo (Hashitossicosi) o di tireotossicosi (nella tiroidite silente) dovuta al rilascio di ormoni tiroidei da parte della tiroide distrutta.
Occasionalmente può essere presente un’oftalmopatia simile a quella che si può riscontrare nel morbo di Basedow.
Spesso le tiroiditi croniche si associano ad altre patologie autoimmuni organo e non-organo specifiche (come gastrite cronica atrofica, anemia perniciosa, anemia emolitica autoimmune, ipoparatiroidismo, vitiligine, diabete mellito tipo 1, morbo di Addison, miastenia gravis, celiachia etc.). Questo fenomeno può essere una semplice associazione di patologie autoimmuni o può configurare un quadro più complesso di sindrome polighiandolare autoimmune. (Prenota una visita endocrinologica).
Pertanto nel caso di tiroidite di Hashimoto è sempre opportuno ricercare altri segni o sintomi correlabili ad altre patologie autoimmuni eventualmente associate.
Inoltre, le tiroiditi croniche potrebbero avere un maggior rischio di sviluppo di neoplasie quali il carcinoma differenziato della tiroide e il linfoma. Pertanto va sempre sospettato lo sviluppo di una neoplasia tiroidea in un paziente con tiroidite cronica, in cui, in corso di terapia sostitutiva, si osserva la comparsa di un nodulo o se il volume ghiandolare aumenta rapidamente. Va ricordato, però, che la presenza di tiroidite di Hashimoto è un fattore prognostico favorevole in un paziente con un carcinoma papillifero. (Prenota una visita endocrinologica).
Diagnosi
La diagnosi si basa su dati di laboratorio che evidenziano la presenza di elevati valori di anticorpi antitiroide associati ad una funzionalità tiroidea che può essere estremamente variabile in base allo stadio della malattia (normale funzione tiroidea; ipotiroidismo subclinico; ipotiroidismo clinico; ipertiroidismo transitorio). L’assenza degli autoanticorpi è un’evenienza rara (5%).
E in tal caso la diagnosi deve essere sostenuta dal quadro ecografico e/o dal citoaspirato.
Inoltre, gli anticorpi anti tiroide che, nella tiroidite di Hashimoto sono presenti a titoli elevati, possono essere presenti, però, con titoli più bassi, anche in soggetti non affetti da tiroidite cronica. Negli adolescenti affetti da tiroidite cronica, inoltre, il livello degli anticorpi anti-tiroide può non essere così elevato e pertanto la diagnosi può essere più difficile.
Normalmente nella tiroidite di Hashimoto gli anticorpi anti TPO sono presenti molto piu’ frequentemente che quelli anti tireoglobulina.
L’esame ecografico può essere d’aiuto nell’evidenziare un quadro di tipo infiammatorio, ipoecogeno e disomogeneo (prenota un’ecografia tiroidea), mentre, l’agoaspirato può essere utile soprattutto nella valutazione di noduli e nella diagnosi differenziale di queste lesioni con le neoplasie della tiroide e i linfomi tiroidei (prenota un agoaspirato tiroideo).
La curva di captazione e la scintigrafia tiroidea non sono utili nella diagnostica della tiroidite cronica.
Terapia
In molti casi non è richiesto nessun trattamento perchè il gozzo è piccolo e il paziente è spesso asintomatico, con livelli di TSH nel range di norma.
Il trattamento sostitutivo con LT4 è obbligatorio quando: 1) viene riscontrato ipotiroidismo franco; 2) in caso di ipotiroidismo subclinico con TSH > 10 U/l ; 3) nelle donne che stanno per iniziare un gravidanza o nei bambini.
Il trattamento sostitutivo con LT4 è consigliato, invece, in soggetti con TSH di 4-10 U/l se hanno gozzo o disturbi clinici riferibili all’ipotiroidismo (astenia, obesita’, dislipidemia), perchè è dimostrato il miglioramento di diversi parametri clinici (performance mentale, contrattilità cardiaca, assetto lipidico) in corso di terapia con LT4.
La terapia non e’ invece obbligatoria negli altri casi con TSH normale o TSH appena al di sopra della norma.
Il trattamento deve mirare a riportare il TSH a valori compresi fra 1 e 2 U/l. Il primo controllo va effettuato dopo 1 mese dall’ inizio della terapia; una volta raggiunto il compenso terapeutico e’ sufficiente monitorare FT3, FT4 e TSH ogni 6-12 mesi.
Durante la terapia nel 50-90% dei casi vi è una riduzione del volume e della consistenza del gozzo, sia per la normalizzazione dl TSH, sia per la riduzione dell’ infiltrazione linfocitaria. Si assiste, solitamente, anche ad una riduzione del titolo anticorpale a cui sembra contribuire una terapia integrativa con selenio.
Il trattamento con levotiroxina è consigliato, quindi, nel caso di gozzo che comprime la strutture adiacenti. Questo trattamento è efficace se il gozzo è di recente riscontro, mentre potrebbe dare scarsi risultati in un gozzo di vecchia data in cui si è già instaurato un certo grado di fibrosi irreversibile. (Prenota una visita endocrinologica).
Sebbene si tratti di una patologia autoimmune, il trattamento steroideo è sconsigliato per via degli effetti collaterali e in quanto non associato ad un reale vantaggio terapeutico
Il trattamento chirurgico, invece, va intrapreso quando i sintomi compressivi permangono nonostante la terapia sostitutiva con LT4 o quando vi è il sospetto di neoplasia.
TIROIDITE SILENTE SPORADICA
E’ detta anche painless perchè l’infiammazione della tiroide avviene in assenza completa del dolore.
Come la tiroidite cronica, questa patologia colpisce prevalentemente le donne.
Sia la patogenesi autoimmune che l’anatomia patologica sono simili a quella della tiroidite di Hashimoto, anche se le cellule oncocitarie si osservano più raramente e la fibrosi e l’atrofia sono addirittura quasi assenti.
Dal punto di vista clinico, invece, si discosta dalla tiroidite cronica di Hashimoto, poichè assume il caratteristico andamento trifasico della tiroidite sub-acuta e della tiroidite postpartum, pur in assenza della caratteristica sintomatologia dolorosa. Da queste ultime due, però, si differenzia perchè il paziente non ha avuto nè una virosi nè una gravidanza.
La diagnosi, quindi, si basa sul riscontro di parametri laboratoristici variabili in base alla fase in cui sono stati eseguiti. Gli anticorpi sono solitamente presenti, anche se non a titoli elevati, mentre il quadro scintigrafico mostra una ridotta captazione da parte della tiroide come nella tiroidite subacuta.
Si tratta quindi di una patologia che assume delle caratteristiche intermedie tra la tiroidite subacuta (con cui condivide manifestazioni cliniche (ad eccezione del dolore) e modalità terapeutiche) e la tiroidite di Hashimoto (con cui condivide patogenesi e anatomia patologica). (Prenota una visita endocrinologica).
La terapia è simile a quella della tiroidite subacuta; pertanto durante la fase tireotossica non è indicato il trattamento con tionamidi, perchè la tireotossicosi e’ causata ad un aumentato rilascio di ormoni e non da una reale iperfunzione tiroidea. Nei casi in cui la sintomatologia sia importante potrebbe essere utile la somministrazione di beta-bloccanti. Nella fase di ipotiroidismo transitorio solitamente non è richiesta alcuna terapia sostitutiva.
TIROIDITE POST PARTUM
E’ una disfunzione che insorge entro un anno dal parto e colpisce mediamente il 5% delle donne. La frequenza sale al 20% nelle donne che hanno un diabete mellito di tipo 1, per motivi di predisposizione genetica.
Fattori di rischio per lo sviluppo di tiroidite post partum sono: 1) storia di precedente tiroidite post partum; 2) anamnesi familiare positiva per distiroidismi; 3) positività degli anticorpi anti tiroide (ma solamente il 50% delle donne con positività anticorpale svilupperà una tiroidite post partum); 4) condizione di fumatrice; 5) presenza di gozzo; 6) eccessivo introito di iodio; 7) presenza di diabete mellito tipo 1.
Il meccanismo patogenetico della tiroidite post partum consiste nel fatto che durante la gravidanza nella donna si sviluppa uno stato di depressione immunologica, che raggiunge il massimo verso il l’ultimo trimestre, tanto che si assiste alla riduzione del titolo anticorpale e della infiltrazione linfocitaria tiroidea. Dopo il parto, si ha una netta riduzione della tolleranza immunologica, anzi si compare un vero e proprio rebound immunologico con inasprimento dei fenomeni autoimmunitari. In questo contesto va inserita la tiroidite post partum, con accentuazione della infiltrazione linfocitaria e con innalzamento degli autoanticorpi a livelli addirittura superiori a quelli presenti prima della gravidanza.
Anche nella tiroidite post partum si assiste al caratteristico andamento trifasico della tiroidite di De Quervain. La prima fase è quella tireotossica, inizia cira 1-2 mesi dopo il parto e può durare per 1-2 mesi. L’ aumento degli ormoni tiroidei in circolo e’dovuto ad un aumentato rilascio da parte dei follicoli danneggiati dal processo infiammatorio riacutizzato. Solitamente, comunque, i pazienti hanno solo lievi sintomi di ipertiroidismo. La seconda fase è quella ipotiroidea, con comparsa di sintomi quali astenia, depressione, gozzo che possono facilmente essere scambiati con quelli comunemente nel post partum. La terza fase è quella del recupero funzionale; solitamente circa il 50% delle pazienti rimane ipotiroidea, l’altra metà, invece, ritorna eutiroidea anche se tenderà a sviluppare un ipotiroidismo permanente nei 3-4 anni successivi o nelle gravidanze successive.
Solitamente il susseguirsi delle tre fasi cliniche è documentabile solo nel 20-30% dei casi, poichè, spesso, alcune di esse possono passare inosservate.
La diagnosi si basa su parametri anamnestici, clinici e laboratoristici che si riscontrano nel post partum.
La terapia è sostanzialmente simile a quella della tiroidite silente; pertanto durante la fase tireotossica non è indicato il trattamento con tionamidi, perchè la tireotossicosi è causata ad un aumentato rilascio di ormoni e non da una reale iperfunzione tiroidea. Nei casi in cui la sintomatologia sia importante potrebbe essere utile la somministrazione di beta-bloccanti. Nella fase di ipotiroidismo transitorio non è richiesta, solitamente, alcuna terapia sostitutiva, a meno che la sintomatologia non sia particolarmente importante; in tal caso deve essere instaurata un terapia sostitutiva per un anno, dopo di che la posologia va gradatamente ridotta al fine di valutare la possibilità di sospenderla completamente. Se l’ipotiroidismo permane, è necessario prolungare la terapia per tutta la vita, se, invece, avviene un ripresa funzionale completa occorre, comunque, monitorare annualmente la paziente perchè rimane a rischio di risviluppare un ipotiroidismo. Elevata (80%) è inoltre la probabilità di sviluppare ipotiroidismo nelle gravidanze successive. (Prenota una visita endocrinologica).
Da evitare, nel frattempo, l’utilizzo di iodio che può favorire lo sviluppo di distiroidismi.
TIROIDITE DI RIEDEL
E’ una malattia molto rara che colpisce prevalentemente le donne di mezza età.
Il meccanismo eziopatogenetico è sconosciuto anche se si pensa che sia lo stesso della tiroidite di Hashimoto, tanto che da alcuni autori è considerata una forma avanzata di tiroidite cronica. Secondo altri, invece, rappresenta un’ entità a sé stante ad eziologia sconosciuta.
Questa tiroidite è caratterizzata da fibrosi della ghiandola tiroidea e delle strutture adiacenti che può decorrere in modo isolato o associata a fibrosi retro peritoneale, mediastinica e delle vie biliari. Nei tessuti fibrotici è stata dimostrata la presenza di eosinofili a conferma della probabile patogenesi autoimmune della patologia.
I sintomi compaiono, solitamente, in modo subdolo e consistono nella comparsa di un gozzo di consistenza duro lignea (che pone sempre dei problemi di diagnosi differenziale il carcinoma tiroideo, ma i linfonodi del collo non sono, solitamente, aumentati di volume) che spesso comprime la strutture adiacenti (trachea, esofago, nervi laringei) causando dispnea, disfagia e disfonia. Il tessuto fibroso, a volte, puo’ infiltrare anche le strutture vascolari viciniori (giugulari, carotidi) e i tessuti muscolari sovrapposti.
La temperatura e gli altri indici infiammatori (VES, i leucociti) sono nella norma.
La funzione tiroidea è normale nel 64% dei casi, è presente ipotiroidismo nel 32% e ipertiroidismo nel 4%. Lo sviluppo di severo ipotiroidismo è raro, ma può verificarsi soprattutto nelle tiroidite di Riedel di vecchia data. Spesso ad essa si accompagna anche un ipoparatiroidismo.
La diagnosi si basa sul dato clinico, sul riscontro laboratoristico di ipotirodismo con anticorpi negativi (o se positivi, a titoli nettamente inferiori a quelli che si riscontrano nella tiroidite di Hashimoto).
La scintigrafia, solitamente, mostra assenza di accumulo di tracciante.
La terapia e’ chirurgica e la tiroidectomia totale sarebbe l’intervento di elezione, anche se spesso è un intervento non realizzabile per la mancanza di piani di clivaggio dovuta alle tenaci aderenze della ghiandola con le strutture circostanti. (Prenota una visita chirurgica). Si ricorre spesso, quindi, alla istmectomia al fine di lateralizzare i due lobi tiroidei e ridurre la compressione sulla trachea. A volte può essere necessaria la tracheostomia. Dopo l’intervento chirurgico è utile la somministrazione di corticosteroidi ad alte dosi (80-100 mg di pednisone per 2-3 settimane e poi a scalare per 6 mesi) per ridurre la reazione fibrotica. Per alcuni, però, la terapia steroidea non sembra modificare l’andamento della malattia.
Recentemente è stato utilizzato, con buoni risultati, il Tamoxifene per os (20 mg per due volte al giorno). Questo farmaco agisce stimolando la produzione di TGF-beta che è a sua volta un potente inibitore dei fibroblasti immaturi e delle cellule epiteliali.
Nel caso di ipotiroidismo è indicata la terapia con LT4 a dosi sostitutive. Secondo altri autori, invece, è più indicata a dosi soppressive al fine di ridurre al minimo lo stimolo del TSH sul trofismo del parenchima tiroideo, anche se fibrotico.
La radioterapia non porta risultati significativi, pertanto va presa in considerazione solo dopo il fallimento della terapia chirurgica e farmacologia.
Prenota una visita specialistica endocrinologica in merito a questo argomento.
Dott. Massimiliano Andrioli
Specialista in Endocrinologia e Malattie del Ricambio
Centro EndocrinologiaOggi, Roma
viale Somalia 33A, Roma
tel/fax 0686391386
cell 3337831426
Studio EndocrinologiaOggi, Lecce
via Ruffano 4, Casarano (Lecce)
tel/fax 0686391386
cell 3337831426
Bibliografia
1) Betterle C, Girelli M E. Tiroiditi. L’ Endocrinologo 2002 Giugno Vol 3, n 2
2) P Reed Larsen, Terry F Davies. Hypothyroidism and thyroiditis. Williams Textbook of Endocrinology 10th Ed, 2002, section three
3) D’Armiento, Screpoli, Attanasio, Graziano, Fumarola. Tiroiditi acute, subacute e croniche Manuale di Terapia delle Malattie Endocrine e Metaboliche, 2000 Andreani, Tamburano
Share
GIU
2011
